Onderscheid tussen natuurlijke en synthetische moleculen
Anno 2021 maakt de wetenschap (zeer) weinig tot geen onderscheid tussen natuurlijke en synthetische moleculen. Toch zijn er meer en meer voorbeelden van het feit dat synthetische moleculen een andere uitwerking hebben wanneer ze in het menselijk lichaam opgenomen worden.
Bijvoorbeeld bij diethylstilbestrol (DES), de synthetische vorm van het vrouwelijke oestrogeen dat in het vrouwenlichaam belangrijke taken vervult, geeft het toedienen aanleiding tot (borst)kanker en genetische afwijkingen bij de nakomelingen en dat minstens tot in de derde generatie. Dit doorgeven over een generatie heen betekent dat de inwerking van de synthetische molecule zo ingrijpend is dat het er op lijkt dat ze in staat is om de genetische overdracht aan te tasten.
Vitamine D is ook een goed voorbeeld. Je kan op 3 manieren je lichaamsvoorraad aanvullen: door in de zon te lopen, via de voeding en door supplementen te nemen. Enkel op de derde wijze kan vitamine D zich in je lichaam opstapelen. Hoe kan dat? Heeft de oorsprong van de supplementen er mee te maken? Het Nederlandse vitamine bureau geeft toe dat er een verschil tussen de opname van natuurlijke en synthetische vitamines kan zijn; en toch laat de EU niet langer toe dat de oorsprong van de vitamines vermeld wordt op de verpakking.
Deze voorbeelden geven een duidelijk signaal van het feit dat we met de huidige wetenschap (en politiek) iets over het hoofd zien.
Welke verschillen zijn er mogelijk tussen chemisch gelijkwaardige moleculen?
Chiraliteit
Een eerste punt van onderscheid tussen chemische en natuurlijke eiwitten is de chiraliteit. Veel organische moleculen kunnen geometrisch gespiegeld worden. In de natuur is er echter meestal maar één van de verschillende configuraties (driedimensionale structuur) aanwezig en bruikbaar. Het chemische spiegelbeeld is meestal giftig! In het tijdschrift “Mens en molecule” (jan 2020 p 30) lezen we het volgende:
“Citronellal, bekend van de etherische olie citronella, komt voor in twee verschillende driedimensionale configuraties: de ene ruikt naar sinaasappel, de ander naar citroen. De twee zijn spiegelbeeld isomeren of enantiomeren van elkaar. Fysisch-chemisch zijn ze aan elkaar gelijk, maar biologisch gezien verschillen ze als dag en nacht. Dat het in de farmaceutische industrie van belang is om optische isomeren van elkaar te scheiden, blijkt wel uit het Softenon-schandaal in de jaren zeventig van de vorige eeuw. Een enantiomeer wist bij zwangere vrouwen inderdaad de misselijkheid te verminderen, het andere veroorzaakte ernstige geboortedefecten.”
Een ander voorbeeld van waar het mis gaat ten gevolge van de verkeerde chiraliteit van een deel van de synthetische moleculen, is in de zenuwcellen. Daar worden deze moleculen als onbruikbaar bestempeld en opgeslagen in de dopamine cellen. Deze opgestapelde moleculen zijn niet enkel onbruikbaar, ze blijken ook giftig te zijn en daardoor de oorzaak van het vroegtijdig afsterven van de cel. Bijzonder hierbij is, dat deze foutief gevouwen eiwitten - nadat ze de cel hebben ziek gemaakt - de zieke cel verlaten - men noemt ze dan ‘prionen’ - en vervolgens binnendringen in gezonde zenuwcellen die op hun beurt ziek worden. Dit is de oorzaak van allerlei zenuwziektes, waaronder de ziekte van Parkinson en Alzheimer. Deze foutief gevouwen eiwitten worden ‘inferieure moleculen’ of ‘prionen’ genoemd.
Merkwaardig hierbij is dat Wikipedia deze eiwitten met een verkeerde chiraliteit in eerste instantie bestempelt als “normale eiwitten”, pas verderop in het artikel wordt de verkeerde chiraliteit vernoemd.
Voor zover bekend is het probleem met prionen voor de mens aan 1 enzymen gelinkt: het normale eiwit PrPc dat wordt gecodeerd door het PRNP-gen (het prionproteïne-gen), is bij de mens gelegen is op chromosoom 20 (locus 20p13). Het ziekteverwekkende eiwit heeft de naam PrPsc. (red 2, 3 & 4)
Er zijn twee manieren waarop het ziekteverwekkende eiwit kan ontstaan. Een: het wordt verkeerd gemaakt in ons lichaam, of twee: het is een reactie op iets wat ons lichaam binnen komt.
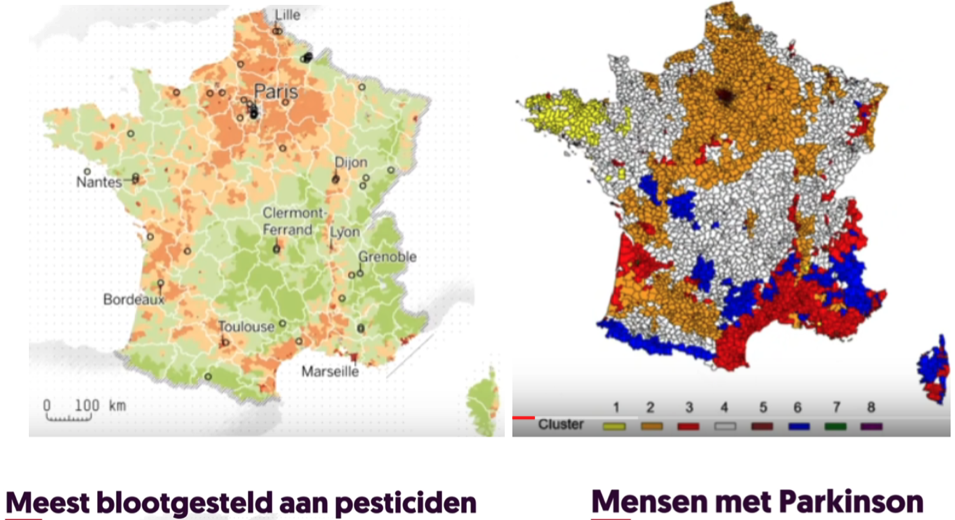
Van alle mogelijke oorzaken van de ziekte van Parkinson, die veroorzaakt wordt door deze prionen, heeft vervuiling voorlopig (2020) het grootste aandeel. Waarschijnlijk komen gifstoffen ons lichaam binnen via het eten en gaan vanuit de darmen, via de Nervus Vagus, naar de hersenen.
In dat verband is het geweten dat boeren een erg verhoogde kans hebben op het ontwikkelen van de ziekte van Parkinson en dit vanwege het gebruik van chemische sproeistoffen. (ref. 1 op minuut 4) Op de kaart van Frankrijk is dit verband duidelijk te zien.
Referenties:
1. ’Waarom krijgt straks iedereen de ziekte van Parkinson?’ https://www.youtube.com/watch?v=3JKECIJDFXUprof dr. Bas Bloem (op minuur6:25)
2. nl.wikipedia.org/wiki/Prion
3. https://nl.wikipedia.org/wiki/Ziekte_van_Creutzfeldt-Jakob#Infectie
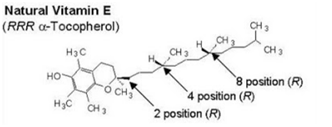
Synthetisch betekent een grote kans op een verkeerde configuratie
De molecule die we vitamine E noemen heeft meerdere ongewenste β-vormen: in de staart van de molecule kan er op drie plaatsen een andere richting aangenomen worden door een deelmolecule. Hierdoor kan de globale molecule, hoewel chemisch identiek, 8 verschillende configuraties hebben.
De biologische processen in ons lichaam (en dat van flora en fauna) onderscheiden de verschillende vormen wel! En om die reden worden in de natuur zowel de chiraliteit als de geometrische structuren bepaald door chaperones (nl-chaperone-eiwitten) Deze eiwitten zorgen voor het juist vouwen van de geproduceerde aminozuren.
“One major function of chaperones is to prevent both newly synthesised polypeptide chains and assembled subunits from aggregating into nonfunctional structures.” (vertaling: Een belangrijke functie van chaperones is om te voorkomen dat zowel nieuw gesynthetiseerde polypeptideketens als geassembleerde subeenheden, zich samenvoegen tot niet-functionele structuren.) De chapereone-functie bestaat niet in het synthetisch productieproces van polypeptiden. Als het gaat over chiraliteit, kunnen we er van uitgaan dat er ongeveer evenveel linkse als rechtse moleculen geproduceerd worden zonder het gebruik van chaperones. Volgens bovenstaande quote zijn de verkeerd gevouwde structuren: “non-functional structures” ofwel “structuren zonder functie”. Ze hebben dan misschien geen functie, ze zijn echter wel chemisch actief – zij het op een verkeerde wijze - in een biologische omgeving en dat maakt ze tot gifstoffen omdat er in de opbouw van de cellen niet gerekend is met het bestaan van deze stoffen.
Met het bovenstaande statement uit wikipedia wordt eigenlijk het verschil tussen natuurlijke en synthetische moleculen toegegeven.
Isotopen
Vervolgens is er de mogelijkheid dat in de natuurlijke opbouw van moleculen, een voorkeur is voor bepaalde isotopen. Er zijn verschillende voorbeelden in de natuur waar geurmolecules met verschillende isotopen onderscheiden worden. Ook bij de selectie van aminozuren wordt een onderscheid gemaakt door levende organismen. In een cel worden proteïnen gemaakt door aminozuur per aminozuur de lange moleculeketens op te bouwen. Zowel dit proces als de aanvoer van de nodige aminozuren worden gestuurd door subtiele krachten die onderscheid kunnen maken tussen aminozuren met verschillende isotopen.
In de synthetische opbouw van dit soort moleculen wordt groffer te werk gegaan. Veelal brengt men halve moleculen bij elkaar die via een chemische reactie aminozuren vormen.
Een bekend voorbeeld van de subtiele selectie van moleculen is aanvoer van zuurstof door hemoglobine. Zowel het opnemen van zuurstof in de longen als het afgeven van zuurstof aan de cel die een zuurstofmolecule nodig heeft, gaat gepaard met de zuurtegraad van het bloed ter plekke (dit heeft te maken met de aanwezigheid van CO2 op die plaats. In principe heeft de zuurtegraad van de omgeving niets te maken met een zuurstofatoom, maar net daarom kunnen kleine verschillen in zuurtegraad kleine verschillen in atomen opmerken en hierdoor een selectie maken. Dit zowel bij de opname uit de buitenwereld (lucht, drank of voedsel) als bij de opname intern... Mogelijk gaat het hier om zaken die wij nog niet kennen of kunnen onderscheiden.
In dit opzicht is het nuttig het werk van Alexander Berezin te vermelden. Hij schreef al een en ander over isotopen in een biologische omgeving. Zijn betoog (in het tijdschrif Nexus aug-seot 2019 pag 45 e.v.) begint bij de samenstelling van de verschillende atomen. Atomen bestaan uit een kern en daar rond cirkelende elektronen. Naar de massa gezien heeft de kern de absolute overmacht in dit systeem. De kern bestaat uit protonen en neutronen. En daar hebben de neutronen dan weer het overwicht: 60%. De ongeveer 80 stabiele elementen die we kennen hebben samen 254 stabiele isotopen. Er zijn echter ongeveer 2400 radioactieve isotopen (natuurlijke en artificiële) bekend. Dat heeft tot gevolg dat er in ieder van ons een grote verscheidenheid aan isotopen is te vinden, en dat heeft dan weer tot gevolg dat we, vanuit ons lichaam, ongeveer 4000 acties van radioactief verval per seconde mogen verwachten. Berezin stelt dat het verval van 14C en 40K (bètaverval) energetisch genoeg is om onze om onze geestelijke en psychologische toestand te beïnvloeden. Bovendien vervalt 14 C naar 14N en 40K naar 40Ca en daarmee transmuteren deze elementen.
Ironisch genoeg gaat Berezin nog verder en wil hij de status van het “Gods”-deeltje van het Higgsboson wegnemen aan het neutron toekennen. Daar voert hij eerst het argument van de te verwachten leeftijd (vervaltijd) voor aan. Maar ook het feit dat het neutron na die tijd vervalt in 3 verschillende deeltjes: een proton, een elektron en een elektron-antineutrino.
Voor het onderwerp van dit artikel wordt het interessant als Berezin stelt dat de verschillende isotopen van één element weliswaar chemisch dezelfde eigenschappen hebben, maar dat ze toch verschillen op basis van een aantal fysische eigenschappen: massa, het magnetisch moment van de kern en trillingsfrequentie wanneer het atoom in een kristal opgenomen is.
Als we ons vervolgens realiseren dat het DNA bestaat uit 5 chemische elementen: waterstof (H), zuurstof (O), koolstof (C), stikstof (N) en fosfor (P) en dat hiervan enkel fosfor maar 1 stabiele isotoop heeft (H, C & N twee isotopen en O drie), dan kunnen we niet anders dan ons afvragen of deze isotopen een meerwaarde kunnen creëren in het informatiebestand van het DNA.
Hierdoor kan de diversiteit van isotopen, de verdeling van isotopen en de zelforganisatie van isotopen leiden tot het fenomeen “isotopiciteit” - studie van de invloed van isotopen.
Nemen we als voorbeeld het belangrijkste element voor het leven: koolstof. Dit heeft twee stabiele isotopen: 12C (99%) en 13C (1%)
Een klein stukje DNA van minder dan 1 micron groot, bevat ongeveer 1.000.000 koolstofatomen. Daarvan zijn statistisch 10.000 13C-isotopen. Die kan je op 1024000 plaatsen tussen de andere koolstofatomen zetten. Wetende dat het heelal tussen de 1080 en 10100 atomen bevat, is de winst aan informatie door het onderscheiden van de 13C fenomenaal.
Samen met de andere isotopen wordt de winst enkel maar groter.
Kwantumverstrengeling
Dan is er het merkwaardige verschijnsel kwantumverstrengeling. Steeds meer voorbeelden van dit verschijnsel duiken op; het fenomeen is dus niet langer te ontkennen. Maar het mechanisme is verre van begrepen: twee of meer natuurkundige objecten kunnen zodanig verbonden zijn, dat het ene object niet meer volledig beschreven kan worden zonder het andere specifiek te noemen - ook al zijn de beide objecten ruimtelijk gescheiden (non-lokaliteit). Bovendien is de scheiding niet enkel ruimtelijk, maar ook in de tijd waargenomen (gelijktijdigheid).
Dit wil zeggen dat eender welke stof aspecten van haar voorgeschiedenis kan meedragen en dat zou wel eens een groot verschil kunnen te vinden zijn tussen synthetisch en biologisch gevormde moleculen. Recentelijk werd hierover een artikel gepubliceerd op Researchgate waarin het bestaan van verbindingen die de ruimte en de tijd overstijgen aangetoond wordt. Deze verbindingen ontstaan via C-zones (Connectie-zones) die verantwoordelijk kunnen zijn voor verregaande vormen van zelforganisatie van de materie. C-zones ontstaan o.a. wanneer er een hoge mate van onrust is in de materie. In de jaren 60 van de vorige eeuw heeft Ilya Prigogine de basis gelegd voor deze waarneming met zijn dissipatieve structuren. In het voornoemde artikel werden verscheidene voorbeelden uit de biologie aangehaald. Natuurlijke moleculen zoals DNA kunnen functioneren als C-zone en zodoende informatie uit de omgeving verwerven door Non-Lokaliteit en via nog een andere eigenschap namelijk Gelijktijdigheid. Synthetische moleculen zijn te star waardoor ze zelf niet kunnen functioneren als C-zones en er ook niet in participeren.
Besluit
Hoewel er nog heel wat onderzoek nodig is om volledig te begrijpen wat het verschil is tussen chemische en biologische moleculen, mag men er om bovenstaande redenen van uitgaan dat chemische moleculen niet hoeven te werken op de wijze van lichaamseigen en natuurlijke moleculen, of niet te onderschatten bijwerkingen op levende wezens kunnen hebben.
We mogen er van uitgaan dat de fine tuning van de chemie van het leven veel dieper gaat dan wat wij anno 2021 beseffen.

